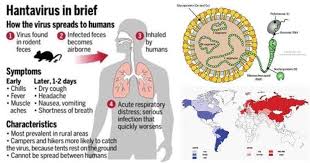
ویروسهای هانتا گروهی از عوامل بیماریزای مشترک میان انسان و حیوان هستند که در سراسر جهان پراکندهاند و میتوانند دو نشانگان بالینی متمایز و بالقوه مرگبار را در انسان ایجاد کنند. این ویروسها که در طبیعت به طور مزمن و بدون علامت، جوندگان وحشی و اهلی را آلوده میسازند، از طریق استنشاق ذرات آلوده به فضولات خشکشده این حیوانات به انسان سرایت میکنند. برخلاف بسیاری از عوامل ویروسی تنفسی، انتقال انسانبهانسان در مورد اکثر هانتاویروسها نادر است، هرچند استثنایی مهم در آمریکای جنوبی وجود دارد که ابعاد نگرانکنندهای به این عفونت بخشیده است. شناخت دقیق این ویروس، مسیرهای انتقال، جلوههای بالینی و راهبردهای پیشگیری، نه تنها برای جوامع در معرض خطر، بلکه برای نظامهای بهداشت عمومی که با چالش بیماریهای بازپدید و نوپدید روبهرو هستند، اهمیتی حیاتی دارد.
هانتاویروسها اعضای خانواده ویروسی هانتاویریده را تشکیل میدهند که خود به راسته بانیاویرالس تعلق دارد. ژنوم آنها از سه قطعه آر.ان.ای تکرشتهای با قطبیت منفی تشکیل شده است که پروتئینهای نوکلئوکپسید، گلیکوپروتئینهای سطحی و آنزیم آر.ان.ای پلیمراز وابسته به آر.ان.ای را کد میکند. برخلاف اغلب بانیاویروسها که از طریق بندپایان منتقل میشوند، هانتاویروسها میزبانهای اختصاصی خود را در میان پستانداران کوچک، بهویژه جوندگان یافتهاند و هر گونه ویروس معمولاً با یک گونه خاص از جونده همزیستی تکاملی طولانیمدتی دارد. برای نمونه، ویروس هانتاان از موش صحرایی راهراه کرهای، ویروس پومالا از موش حشرهخوار جنگلی اروپایی، ویروس سین نومبره از موش آهوی شمال آمریکا و ویروس آند از موش برنجخور دمبلند در آمریکای جنوبی جدا شدهاند. این اختصاصیت میزبانی، پراکندگی جغرافیایی بیماری را نیز شکل میدهد و بر اساس منشأ تکاملی، هانتاویروسها را به دو گروه عمده «جهان قدیم» (اروپا و آسیا) و «جهان جدید» (قاره آمریکا) تقسیم میکند.
ویروسهای جهان قدیم عمدتاً با ایجاد تب خونریزیدهنده همراه با سندرم کلیوی شناخته میشوند. این بیماری که برای دههها با نامهای تب خونریزیدهنده کرهای، نفروپاتی اپیدمیک و بیماری مشابه در بالکان و روسیه گزارش میشد، طیفی از شدت را بروز میدهد. دوره کمون معمولاً بین یک تا شش هفته طول میکشد و شروع ناگهانی علائمی چون تب بالا، لرز، سردرد شدید، درد شکم و کمر، تاری دید و برافروختگی صورت، بهویژه در ناحیه گونهها و چشمها، به چشم میخورد. تظاهرات خونریزیدهنده که از پتشی و خونریزی زیر ملتحمه تا خونریزیهای گوارشی و حتی داخل جمجمهای متغیر است، در فاز دوم بیماری پدیدار میشود. مشخصه اصلی این نشانگان، درگیری کلیوی است که به صورت کاهش ناگهانی حجم ادرار و افزایش سریع کراتینین سرم تظاهر میکند و ممکن است به نارسایی حاد کلیه نیازمند دیالیز منجر شود. پس از چند روز افت فشار خون که میتواند به شوک بینجامد، مرحله پرادراری آغاز میشود و در صورت بقای بیمار، عملکرد کلیوی به تدریج طی هفتهها تا ماهها بهبود مییابد. گونههای مختلف جهان قدیم شدتهای متفاوتی دارند: ویروس هانتاان و دبراوا مرگومیر ۵ تا ۱۵ درصدی را سبب میشوند، حال آنکه ویروس پومالا فرم خفیفتری به نام نفروپاتی اپیدمیک ایجاد میکند که میزان مرگ آن کمتر از یک درصد است.
در مقابل، هانتاویروسهای جهان جدید عمدتاً ریهها را هدف قرار میدهند و موجب سندرم ریوی هانتاویروس میشوند که نخستین بار در سال ۱۹۹۳ در منطقه چهار گوشه ایالات متحده شناسایی شد. این بیماری نیز با دورهای شبهآنفلوآنزا شامل تب، خستگی مفرط، درد عضلانی بهویژه در رانها و کمر، و گاه علائم گوارشی مانند تهوع و اسهال آغاز میشود. اما آنچه این سندرم را مرگبار میسازد، گذار ناگهانی به فاز قلبیریوی است که طی آن نشت گسترده مویرگهای ریوی، مایع را به درون کیسههای هوایی سرازیر میکند و تصویری شبیه به ادم ریوی غیرقلبی یا سندرم دیسترس تنفسی حاد ایجاد مینماید. بیمار طی ۲۴ تا ۴۸ ساعت دچار تنگی نفس پیشرونده، سرفه خشک و افت شدید اکسیژن خون میشود و بدون مداخله فوری تنفسی، نارسایی چندارگانی و مرگ رخ میدهد. میزان مرگومیر سندرم ریوی هانتاویروس بسته به عامل ویروسی و سرعت دسترسی به مراقبتهای ویژه بین ۳۰ تا ۵۰ درصد متغیر است. ویروس سین نومبره شایعترین عامل در آمریکای شمالی است، حال آنکه ویروس آند در آمریکای جنوبی گذشته از ایجاد فرم شدید بیماری، ویژگی منحصربهفردی دارد: این تنها هانتاویروسی است که انتقال انسانبهانسان آن از طریق تماس نزدیک با فرد علامتدار، بهویژه در میان اعضای خانواده و کارکنان بهداشتی، اثبات شده است و نگرانی از گسترش فراتر از کانونهای محدود را دامن میزند.
انتقال ویروس به انسان تقریباً منحصراً از طریق استنشاق آئروسلهای حاوی ویروس از ادرار، مدفوع یا بزاق خشکشده جوندگان آلوده صورت میگیرد. این حالت بهویژه هنگام جارو زدن یا تمیزکاری فضاهای بستهای که مدتها میزبان جوندگان بودهاند، مانند انبارها، کابینهای جنگلی، طویلهها و خودروهای رهاشده، رخ میدهد. گزش جونده و تماس مستقیم مخاط با اشیای آلوده نیز راههای نادرترند، اما ناقلهای بندپا نقشی ندارند. خوشبختانه ویروسها در محیط بیرون بهسرعت با نور فرابنفش و خشکی غیرفعال میشوند، اما در فضاهای تاریک و مرطوب میتوانند چند روز تا چند هفته عفونتزا باقی بمانند. نوسانات جمعیت جوندگان که خود تحت تأثیر عوامل اقلیمی مانند پدیده النینو، بارندگی فراوان و وفور منابع غذایی قرار دارد، مستقیماً بر بروز اپیدمیهای منطقهای اثر میگذارد.
تشخیص زودهنگام عفونت هانتاویروس با چالش بزرگی همراه است، زیرا علائم اولیه غیراختصاصی و مشابه بسیاری از بیماریهای ویروسی شایع است. در عمل بالینی، ظن قوی باید بر اساس شرح حال تماس احتمالی با جوندگان یا فضاهای آلوده شکل گیرد و تستهای آزمایشگاهی اختصاصی بهکار گرفته شوند. روش استاندارد، سرولوژی با الایزا برای شناسایی آنتیبادیهای IgM و IgG ضد هانتاویروس است که در اکثر بیماران در زمان بستری قابل تشخیص است. واکنش زنجیرهای پلیمراز رونویسی معکوس نیز میتواند آر.ان.ای ویروس را در خون یا بافتها شناسایی کند و ایمونوهیستوشیمی بر روی نمونههای کالبدگشایی به تأیید گذشتهنگر کمک میکند. هرچند تستهای تجاری برای برخی گونهها در دسترس است، اما تنوع آنتیژنیک ویروسها و نیاز به آزمایشگاههای با سطح ایمنی زیستی بالا، توانایی تشخیصی را در بسیاری از مناطق آندمیک محدود میکند.
در حال حاضر هیچ داروی ضدویروسی اختصاصی تأییدشدهای برای درمان هانتاویروس وجود ندارد و واکسن مؤثر و در دسترس جهانی نیز تاکنون تولید نشده است. ریباویرین، یک آنالوگ نوکلئوزیدی با طیف گسترده، در مطالعات اولیه بر تب خونریزیدهنده همراه با سندرم کلیوی امیدبخش بود و تجویز زودهنگام آن در برخی کشورهای آسیایی کاهش شدت بیماری و مرگومیر را نشان داده است، اما کارآزماییهای بالینی بر روی سندرم ریوی هانتاویروس در قاره آمریکا مزیت بقا را تأیید نکردند. بنابراین، سنگ بنای مدیریت بیماران، مراقبتهای حمایتی پرستارانه و پزشکی در بخش مراقبتهای ویژه است. در سندرم ریوی، حفظ اکسیژنرسانی اغلب نیازمند تهویه مکانیکی با فشار مثبت و در موارد مقاوم، بهکارگیری روشهای پیشرفته مانند اکسیژنرسانی غشایی برونپیکری است. در تب خونریزیدهنده، مدیریت دقیق مایعات برای پیشگیری از اضافهبار حجمی در فاز کمادراری و دیالیز بهموقع، حیاتی است. تجویز پلاکت و فرآوردههای خونی نیز ممکن است با توجه به شدت خونریزی نیاز شود. رویکردهای نوین درمانی مانند استفاده از آنتیبادیهای مونوکلونال خنثیکننده و داروهای مهارکننده مسیرهای ایمنیزایی هنوز در مراحل تحقیقاتی قرار دارند.
فقدان درمان قطعی، اهمیت راهبردهای پیشگیری را دوچندان میکند. از آنجا که ذخیره اصلی ویروس جوندگان هستند، محور اصلی پیشگیری، به حداقل رساندن تماس انسان با این حیوانات و ترشحات آنهاست. در منازل و اماکن کاری باید درزها و منافذ بالای یک سانتیمتر مسدود شوند، پسماندهای غذایی سریعاً جمعآوری و از انباشته شدن هیزم و اشیای بیاستفاده در نزدیکی ساختمانها پرهیز گردد. هنگام پاکسازی فضاهای آلوده به مدفوع موش، هرگز نباید از جاروی خشک یا دمندههای هوا استفاده کرد. دستورالعمل استاندارد توصیه میکند که ابتدا محلول ضدعفونیکننده (مانند سفیدکننده خانگی رقیقشده به نسبت یک به ده) بر روی فضولات اسپری شود و پس از گذشت چند دقیقه، با دستکش لاتکس و ماسک استاندارد N95 یا بالاتر، مواد خیس را جمعآوری و بهطور ایمن دفع کرد. اشیای قابل شستوشو نیز باید با ماده ضدعفونیکننده تمیز شوند. در مشاغل پرخطری چون جنگلبانی، کشاورزی و کنترل آفات، استفاده از تجهیزات حفاظت تنفسی مناسب باید اجباری باشد. در زمینه واکسن، کره جنوبی و چین واکسنهای غیرفعال تهیهشده از مغز موش یا کشت سلولی را عمدتاً علیه ویروس هانتاان و سئول در جمعیتهای پرخطر به کار گرفتهاند، اما این واکسنها در سطح بینالمللی تأیید نشدهاند و برای گونههای جهان جدید کارایی ندارند.
از نگاه اپیدمیولوژیک، هانتاویروسها در تمام قارهها به جز جنوبگان حضور دارند و هر سال دهها هزار مورد بیماری، عمدتاً از نوع تب خونریزیدهنده، در اوراسیا گزارش میشود؛ در حالی که موارد سندرم ریوی در آمریکا اگرچه کمتر شایع است، اما به دلیل مرگومیر بالا و ماهیت دراماتیک بالینی، بیشتر در کانون توجه رسانهای و علمی قرار دارد. تغییرات اقلیمی و دگرگونی کاربری زمین، بهواسطه افزایش جمعیت جوندگان و گسترش زیستگاههای مرزی میان انسان و طبیعت، پیشبینی میشود که الگوی رخداد این بیماریها را در دهههای آینده تغییر دهد. از این رو، نظامهای پایش بیماریها باید برنامههای دیدهوری اکولوژیک را برای ردیابی طغیانهای جمعیت جوندگان و آلودگی ویروسی آنها تقویت کنند.
در جمعبندی، ویروسهای هانتا نمونهای گویا از عوامل بیماریزایی هستند که در مرز باریک میان زیستبومهای وحشی و جوامع انسانی کمین کردهاند. آنها یادآوری میکنند که سلامت انسان به شکلی جداییناپذیر با سلامت حیوانات و محیط زیست گره خورده است و رویکرد «سلامت واحد» تنها مسیر پایدار برای پیشگیری و مقابله با این تهدیدهای پنهان به شمار میرود. اگرچه این ویروسها همچنان نادر و محدود به کانونهای خاصی باقی ماندهاند، درسهایی که از شناسایی و مدیریت آنها گرفته میشود – از اهمیت تاریخگیری دقیق شغلی و محیطی تا آمادگی بخشهای مراقبت ویژه و توسعه سریع ظرفیتهای تشخیص مولکولی – سرمایهای بیبدیل برای رویارویی با همهگیریهای آینده است. آگاهی عمومی در کنار آموزش مداوم کادر بهداشتیدرمانی، نخستین و مؤثرترین سد دفاعی در برابر ابتلا به این عفونتهای مرگبار خواهد بود.
تعداد نظرات : 0
هنوز نظری برای این مطلب ثبت نشده است.
ارسال نظر